首例体外受精(IVF)并成功妊娠至今已过去30年。期间IVF技术取得重大突破,比如促排卵方案、取卵技术以及为改善胚胎质量而定制的培养基(Gardner 1988)。然而,IVF女性移植正常发育的胚胎与受孕率之间仍存在差异。尽管选择了看起来正常的胚胎进行移植,但仍有高达85%的胚胎植入失败(Smllam 2002)。这一失败率表明,胚胎移植过程是辅助生殖技术(ART)妊娠成功至关重要的一步(Meldrum 1987)。
胚胎移植传统的操作是通过一根导管在“盲视”下将发育2-5天的胚胎移植到宫腔内。这一技术高度依赖临床医生的技巧和手感。许多临床医生会在距宫颈外口固定距离(6cm)置入胚胎;然而,由于宫颈长度及宫腔形态的差别,通常不能保证最佳的移植位置(Brown 2007)。最近,很多研究提出移植后低妊娠率的潜在相关因素,如子宫收缩,胚胎流产,移植导管头有血块或粘液,导管细菌污染,以及胚胎留存(Schoolcraft 2001)。目前将超声介导的胚胎移植(UGET)作为标准的临床操作,与直接移植相比,它似乎提高了临床妊娠率(Brown 2007)。

(图1)
然而,关于UGET可以提高临床受孕率的实际功效仍然存在争议(Kosmas 1999)。之前有报道,子宫内膜胚胎移植(SEED)技术在增加受孕率的同时,减少与ART相关的异位妊娠 (KAMRAVA 2010)。在这项研究中,我们使用了类似技术,在直视下,用软性微型宫腔镜直接将分裂出4-12细胞的胚胎移植到子宫内膜上。宫腔镜的引导可以确保移植的位置更加精确和可靠。
本报告中包括35名年龄在22岁至46岁之间进行IVF的患者。在进入周期前签署知情同意。使用促卵泡素ß(Follistim®, Organon Pharmaceuticals, Inc. )控制性超促排卵。服用醋酸加尼瑞克(AntagonTM, Organon Pharmaceuticals, Inc.)控制内源性促性腺激素激增(如预防LH的激增)。在门诊局部麻醉和轻微镇静作用下取卵。在37°C和含5%二氧化碳的空气培养箱中,卵母细胞在人类输卵管液的合成培养基中受精并培养。在受精后的48-72小时内移植胚胎。所有女性都接受一定的黄体支持,如孕激素或hCG(取卵后3天和6天 hCG 3000 IU)。血清hCG在末次使用hCG后10天行检测;结果大于5 IU/ml伴月经延迟,确认怀孕。
宫腔镜下胚胎移植(HEED)的简介:
经阴道超声检查,确定子宫腔的方向和子宫内膜的厚度。病人取膀胱截石位,置入阴道窥器暴露宫颈。用改良HAM溶液清洗阴道和宫颈。接着, 10ml 1%利多卡因注射于双侧子宫骶韧带,进行神经末梢阻滞麻醉。
用鼠齿钳夹固定宫颈。氮气作为膨宫介质,通过膨宫机膨涨宫腔。直径3mm的软性宫腔镜 (图1)装上含有胚胎的移植导管(图2),在直视下轻柔通过宫颈外口直接植入宫腔内。在直视下,导管进入宫腔的底部。载有胚胎的移植导管(Precision Reproduction, LA, CA USA) 从宫腔镜顶端向前探出1.5cm,置于胚胎着床的位置,位于双侧输卵管开口连线中间,宫底正中最低点。

(图2)
随后,胚胎学家轻柔地释放胚胎。我们的研究结果显示,宫腔镜下早期胚胎移植获得的较高妊娠率,是盲视下移植率的2-3倍。直视化为胚胎移植提供了一种客观的、可视化的、可重复的技术。使得胚胎移植不过分依赖于操作者的操作技巧,而且不同于常规的胚胎移植,因为后者操作人员的经验可能会影响整体妊娠率的变化(Garcia 2002)。宫腔镜下胚胎移植可能会避免许多已知的和既往报道过的胚胎移植不良预后的相关因素。由于多种病因,导致我们很多病人在尝试IVF-ET之前出现不孕。
一种重量较轻的微型宫腔镜软镜用于子宫腔内膜的观察(Storz®, LA, CA USA )。
这种宫腔镜的远端灵活弯曲,直径3mm,有操作通道。而且,滤光器与光源直接相连,减少了镜体重量,给使用者带来更佳的使用感受。另外,胚胎移植所用导管的尖端呈锥形,且开口为60度斜面(约500μm),由聚碳酸酯制成(Precision Reproduction, LLC, LA, CA USA )。
结果
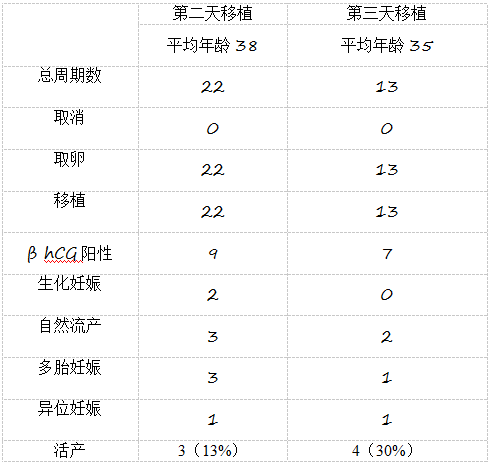
共纳入35个周期,所有都进行了取卵。其中因男方因素,有22个周期进行胞浆内单精子注射(ICSI)。子宫内膜厚度在7到16mm之间,22个周期在第2天移植,13个周期在第3天转移。在胚胎移植12天后,有16个hCG阳性,检测大于5 IU/ml。其中,2例生化妊娠,12例临床妊娠,表现为妊娠5周时超声检查可见妊娠囊,以及妊娠6周时可见胎心。5例妊娠7-8周出现早期流产。7例妊娠至足月分娩健康活婴,2例异位妊娠(表1)。
表1
讨论
正如人们所预期的那样,第3天较第2天移植的患者平均年龄更低(35岁和38岁),因为他们的胚胎质量更好,这使得胚胎可以有机会多培养1天。有意思的是,在第3天移植的妊娠率也更高(31%和15%)。
宫腔镜胚胎移植的优点包括其操作过程的客观性和可重复性。其独特而重要之处在于,通过直视下确认,增加了正确进入宫腔的可靠性。此外,以少量移植介质为载体,将胚胎放置在精确的位置并植入,对患有子宫畸形、肌瘤、腺肌病和宫腔粘连的患者来说,也是有利的。直视下沿宫腔轮廓进行操作,从而降低了子宫内膜损伤的几率。
此外,通过惰性气体(氮气)对子宫进行气体膨胀,导管头端不易与宫底接触,可减少因刺激引起的子宫收缩而导致的不利于移植的环境(Kovacs 1999,Lesny 1998)。据报道,子宫频繁收缩与临床妊娠率低和胚胎流产(Fanch1998)有关。也有人推测,胚胎排出到子宫下段可能会导致宫颈异位妊娠以及胎盘前置(Romundstad 2006; Schoolcraft 2001 )。

临床实践证明,医生可以在宫腔镜下发现子宫收缩,从而中止或推迟手术,这样不仅减少花费,而且能降低多次胚胎移植失败,胚胎损失,以及宫颈异位妊娠和胎盘前置的风险。导管前端的可视化可确保胚胎没有遗留在导管中或丢失。Viser等人发现,移植导管遗留胚胎导致妊娠率较低(3%及20.3%)。此外,导管前端的可视化为胚胎移植提供比常规(30μl)少的移液量(5μl),这样可以更好地将胚胎沿着子宫内膜适当方向放置在稳定的位置。有报道称移液量少可以增加妊娠和着床率(Meldrum 1987)。这也可能有助于降低异位妊娠率,因为有研究显示较大移液量可能增加异位妊娠的风险(Marcus 1995)。确定这种小体积含有胚胎的移液量是否排出,目前只能通过直视的方法。在非直视过程中,人们真正担心的是,在胚胎移植后导管撤出的过程中,这个微小的液滴可以被拖至子宫下段,或进入子宫颈管内或随着导管撤回而移出子宫。
这种技术的潜在缺点和风险是损伤子宫内膜,然而这种风险可能低于盲视下和超声引导下移植对子宫内膜的破坏,因为子宫内膜的可视化以及不需要为了便于超声识别而移动导管(Garcıa-Velasco 2002)。此外,如果出现内膜损伤,可视化还可以将胚胎放置在其他位置。其主要缺点在于宫腔镜检查是一种侵入性的手术。然而,与可能造成子宫创伤的硬性内镜不同,本研究使用的宫腔镜是一个直径3毫米的微型镜体,其具有灵活可弯曲的头端,可很容易随子宫的曲度前行。
使用的导管属于半硬性的,一方面可防止它通过内镜变弯,另一方面它可随内镜弯曲。在我们的研究中,没有发生子宫内膜损伤或子宫出血的情况。费用的增加是它的另一个缺点,但是使用宫腔镜可以减少因多次移植失败产生的费用,并提高患者的满意度。
结论
宫腔镜下子宫内膜胚胎移植(HEED)是一项提高临床妊娠率的有效技术,特别针对IVF-ET反复失败者,这是可行的办法。由于宫腔镜具有可定位和可重复性,能够提高胚胎着床位置的准确度,减少多胎妊娠,使我们将更多精力放在如何提高选择胚胎的能力,使胚胎移植具有较高的生存潜力。通过使用5μl移液量以及直视下确认胚胎位置远离宫角,减少IVF后异位妊娠的机会。通过SEED技术进行囊胚移植,可消除异位妊娠。
(本文译自www.hysteroscopy.info)
-完-
【译者简介】

赵玉婷,女,主治医师,2011年7月毕业于首都医科大学七年制临床医学专业,医学硕士,同年进入首都医科大学附属复兴医院宫腔镜中心工作至今。2015年通过主治医师资格考试,2016年完成北京市住院医师规范化培训二阶段考核。在读首都医科大学妇产科博士,导师首都医科大学附属复兴医院 TinChiu Li 教授,国际知名的生殖医学专家。毕业后一直从事妇产科临床、教学及科研工作,擅长妇科内镜技术、妇科3D超声,女性不孕症、宫腔粘连等疾病的诊治。工作期间发表核心期刊论文1篇。






 2020
2020 